臨床試験においてすべてのリスクを排除する方法はありません。しかし、臨床試験のすべての段階で患者の安全を最大限に高めるための安全策が講じられています。
病状の臨床試験への参加を検討したことがある方は、それが安全なのかどうか疑問に思ったことがあるかもしれません。答えは簡単ではありません。多少のリスクを伴うものもあれば、それ以上のリスクを伴うものもあります。しかし、メリットがリスクを上回る可能性があります。
臨床研究試験は、新しい薬、製品、または手順を人で試験することを目的とした研究です。彼らは次のような質問に答えようとしています。
- この新しい治療法は役に立ちますか?
- そのメリットはリスクを上回りますか?
- この新しいアプローチは、安全に症状を治療または治癒したり、症状を緩和したりできるのでしょうか?
- このアプローチをどのように活用すべきでしょうか?
- この新しい治療法は既存の治療法と比較する場合、どのように比較されますか?
リスクのレベルは、試験と、研究者がどのような製品、サービス、薬剤、または介入を試験しているかによって異なります。
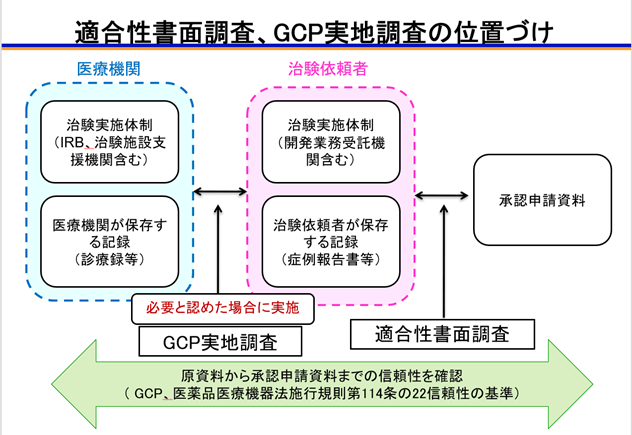
研究者は臨床試験の安全性をどのように確認するのでしょうか?
たとえ軽微であっても、すべてのリスクを排除する方法はありません。しかし、研究者や政府機関がリスクを最小限に抑え、患者の安全を確保しようとする多くの方法があります。
研究者は、政府の規制に従い、次のことによって安全性の確保に貢献します。
- プロトコールと呼ばれる研究計画を作成する
- 治験審査委員会(IRB)の設置
- データおよび安全性監視委員会 (DSMB) の形成
- インフォームドコンセントを得る
- 結果を食品医薬品局 (FDA) に報告する
これらの保護のいくつかを詳しく見てみましょう。
プロトコル
まず、すべての臨床試験には、研究ガイドラインを詳しく説明するプロトコルまたは計画と呼ばれるものがあります。その計画には次のものが含まれます。
- 試験の目的と目標
- 必要なボランティアの種類
- 研究者はどのように研究を行うか
- 治験参加者の安全をどのように監視するのか
- 関連する薬剤、装置、または方法
- 収集する情報の種類
- 裁判はどれくらい続くのか
研究に IRB がある場合、IRB は治験実施計画書を検討し、研究を開始する前に変更を加えたり、ガイダンスを提供したりします。
治験審査委員会
治験審査委員会の仕事は、詳細な研究計画を審査し、承認することです。理事会の目標は、裁判に関係する人々を守ることだ。によると、
- 科学者
- 医師
- 聖職者
- 患者擁護者
IRB の少なくとも 1 人のメンバーは、その施設に所属していない非科学者である必要があります。
治験審査委員会は、治験が合法的で倫理的であり、適切に設計されていることを保証します。また、計画に不必要なリスクが含まれておらず、安全計画が含まれていることも確認します。
臨床研究を行うすべての医療施設には治験審査委員会があります。施設の治験審査委員会は、開始前に各治験を審査します。
しかし、すべての臨床試験に治験審査委員会があるわけではありません。治験に治験審査委員会を設ける必要がある場合については、施設ごとに独自のガイドラインがあります。ただし、一般に、臨床試験が FDA 規制の医薬品、製品、または機器を研究している場合、または連邦政府によって資金提供または実施されている場合、臨床試験には IRB が必要です。
人間研究保護局 (OHRP) は治験審査委員会に指導と監督を提供する場合があります。
DSMB
治験審査委員会に加えて、一部の治験では
DSMB は、特に患者の安全性に焦点を当てて、研究から得られたデータを随時レビューします。 DSMB は IRB よりも多くのデータを確認できるため、安全性をより適切に評価できます。 DSMB は、試験が害を引き起こすという証拠がある場合、試験の中止を推奨できます。
IRB は、DSMB の計画と推奨事項を独自の研究レビューで検討します。
すべての第 3 相(後期)臨床試験
DSMB のすべてのメンバーは独立している必要があります。つまり、彼らは研究機関や研究スポンサーとは一切関係がありません。
インフォームドコンセント
FDA は研究者にインフォームドコンセントを得ることを要求しています。つまり、参加するにはあなたの同意を得る必要があり、次のような治験の詳細をあなたに知らせる必要があります。
- あなたが受ける介入や処置
- 治験計画(プロトコール)とその仕組み
- 起こり得るリスクや不快感
- 参加は任意であるという事実
治験報告
研究者は、特定の種類の臨床研究を、研究とその結果のオンライン データベースである Clinicaltrials.gov に報告する必要があります。国立医学図書館はこのサイトを管理しており、世界中の研究が含まれています。
一般に、研究著者は、米国で行われた研究、または米国の製品に関係する研究である限り、FDA 規制の医薬品、製品、または機器に関する研究について報告する必要があります。
Clinicaltrials.gov には、著者が報告する必要のない研究も多数含まれています。これらには、観察研究や、医薬品や医療機器を調査していない研究が含まれます。ウェブサイトによると、50 州すべてと 221 か国の研究者がデータベースでの研究を報告しています。
臨床試験にはどのようなリスクがありますか?
一部の臨床研究試験では最小限のリスクしか伴いません。他の人はより多くのリスクを抱えている可能性があり、研究主催者は治験が始まる前にリスクを説明する必要があります。
リスクが最小限であるとは、試験中の危害や不快感の可能性が、日常生活で通常経験するものよりも悪くないことを意味します。
最小限の害に加えて、考慮すべき臨床試験の欠点は次のとおりです。
- 治験が研究している介入や製品から利益を得られない可能性があります。
- 研究手順は標準的な医療とは大きく異なる場合があります。
- この研究により、未知のリスクにさらされる可能性があります。
- トライアルに関連して費用が発生する場合があります。

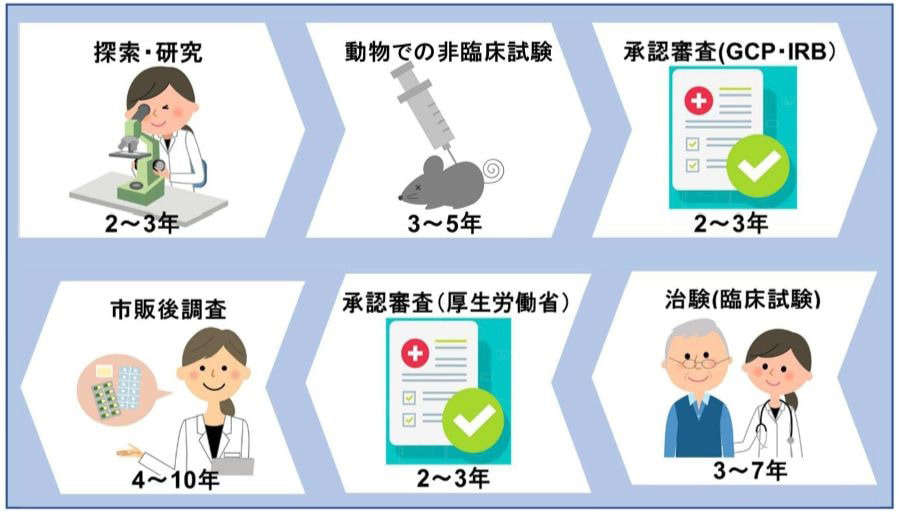
臨床試験の一部のフェーズは他のフェーズよりもリスクが高いですか?
研究者は多くの場合、さまざまな段階で臨床試験を実施します。これは特に実験薬に当てはまります。
フェーズ 1
研究者は、病気や症状のない通常のボランティアの小グループを対象に、新しい薬や治療法を初めてテストします。グループは通常20人から80人程度です。研究者らは介入の安全性を検討し、安全な投与量を見つけ出し、副作用を特定しようとしています。
フェーズ2
病気や症状を抱えた人々を含む、通常は数百人のより大きなグループが投薬や介入を試みます。研究者はこのグループでその安全性を再度評価する予定です。
フェーズ 3
数千人の参加者が新しい治療法を試し、その効果を確認します。サンプルサイズが大きいため、研究者は一般的な副作用のほとんどを特定できます。また、同じ症状に対する他の薬と比較することもあります。
フェーズ4
研究者は、FDA が介入とその公的販売を承認した後、これらの試験を実施します。参加者はさまざまな集団で薬の効果のテストを続け、より多くのデータを取得します。
各段階にはそれぞれのリスクが伴いますが、研究が始まると未知の部分がさらに多くなります。

臨床試験の利点は何ですか?
臨床試験の支持者らは、臨床試験は参加者や病状の治療を必要とする人々に利益をもたらすと主張している。治験は、新しい研究を生み出し、一般的な医療問題に対する解決策の可能性を生み出すのに役立ちます。
参加者はまた、新しい薬や治療法を早期に利用できるという恩恵を受け、より多くの医療ケアや治療を受けることができます。

よくある質問
臨床試験ではプラセボが使用されますか?
はい、一部の臨床試験ではプラセボが使用されています。プラセボとは、有効成分も効果もありませんが、本物の治療法であるように見える錠剤またはその他の介入です。治験に参加している人々は、誰が偽薬を投与されるのか、それとも本物を投与されるのかを知りません。これを盲検といいます。
プラセボを使用すると、研究者は介入の有効性と介入なしの有効性、およびプラセボ効果を比較できます。
私の情報は機密として扱われますか?
研究者が情報を開示できることに書面で同意しない限り、あなたの情報は保護されます。 1996 年医療保険の相互運用性と責任に関する法律 (HIPAA) は、臨床試験中も含めてお客様の情報を保護します。
HIPAA は、機密の患者健康情報を保護するための国家基準を作成する連邦法です。これにより、他人があなたの同意または知らないうちにあなたの情報を開示するのを防ぎます。
研究者が主に研究を支援する目的で、あなたの許可なしにあなたの情報を使用できる限定的かつ狭義の状況があります。保健福祉省 (HHS) のサイトには、例外の詳細なリストが掲載されています。
臨床試験には料金を支払う必要がありますか?
一部の臨床試験では、無料で参加できます。他の人が費用を負担する可能性がありますが、あなたの保険がそれらをカバーする可能性があります。
によると、
- 医療専門家の訪問
- 病院に滞在します
- 標準的ながん治療
- がんの症状を改善したり副作用を軽減したりする治療法
- 臨床検査、X線検査、画像検査
ただし、保険会社は次のような一部の調査費用を負担しない場合があります。
- 研究薬
- 研究目的のみで実施されるテスト
- 研究目的のみの追加の画像処理および X 線撮影
医師に尋ねるべき質問
臨床研究に参加するかどうかを決めるには、多くのことが考慮されます。医療専門家と話し合うべき治験の安全性に関する重要な質問は次のとおりです。
- 研究の目的は何ですか?誰が資金を提供していますか?
- 誰が学習計画を見直しましたか?
- どのような治療、処置、検査を受けることになりますか?
- 私の結果と安全性はどのように監視されますか?
- 研究はどれくらい続きますか?
- この新しい治療法で考えられる短期的および長期的な利点は何ですか?
- この新しい治療法の潜在的な短期的および長期的なリスクは何ですか?
- この研究は、私がすでに受けているケアにどのような影響を及ぼしますか?
- 私のケアは誰が担当してくれるのでしょうか?
- 参加は私の私生活にどのような影響を及ぼしますか (時間や交通の約束、経済的義務など)?
- かかる場合、費用はいくらですか?私の健康保険はそれらをカバーしますか?
- 私の治療法にはどのような選択肢がありますか?

臨床試験に参加するにはどうすればよいですか?
臨床試験への参加を検討している場合は、役立つ簡単なツールがあります。国立医学図書館には、募集中の臨床試験、または今後募集する可能性のある臨床試験を見つけることができる検索ツールがあります。
データベースは条件や国ごとに検索できます。
臨床試験の多様性
臨床試験の結果によって、一般の人々が後でどのような新しい医療介入を受けることができるかが決まります。臨床試験には多くのボランティアがいますが、必ずしも米国の多様な人口を反映しているわけではありません。治験グループは、多くの場合、人種的、民族的、または社会経済的により多様である必要があります。
試験に多様性がないと、健康に影響を与える可能性があります。投薬と介入は、背景や特性が異なる人々にそれぞれ異なる影響を与えます。
だからこそ、
アン

取り除く
臨床試験は、ボランティアが新しい治療法がどれほど効果的かを調べる研究に参加する機会を提供します。政府機関を含むいくつかの団体は、あなたの安全を最優先にするためのルールを定めています。それでも、すべてのリスクを排除することはできません。
試験が異なれば、リスクのレベルも異なります。考えられる利益がリスクを上回るかどうかを判断するには、医療専門家に相談するのが役立ちます。
治験への参加は任意です。ボランティアは白人や年配の方が多い傾向があります。試験の多様性を高めることは、結果の質の向上に役立ちます。
参考文献
- https://medlineplus.gov/clinicaltrials.html
- https://www.fda.gov/media/75398/download
- https://www.hhs.gov/ohrp/index.html
- https://www.cancer.gov/publications/dictionaries/cancer-terms/def/irb
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8617574/
- https://clinicaltrials.gov/
- https://www.nidcr.nih.gov/research/human-subjects-research/toolkit-and-education-materials/interventional-studies/data-and-safety-monitoring-board-guidelines
- https://www.hhs.gov/hipaa/for-professionals/special-topics/research/index.html
- https://www.cancer.gov/about-cancer/treatment/clinical-trials/paying
- https://www.fda.gov/media/143592/download
- https://clinicaltrials.gov/ct2/search
- https://www.fda.gov/consumers/minority-health-and-health-equity-resources/clinical-trial-diversity
臨床試験と安全性: あなたの質問に答えます・関連動画
免責事項: 健康百科事典ブログは、すべての情報が事実に基づき、包括的で最新のものであるよう努めています。しかし、この記事は、資格を持つ医療専門家の知識や専門性の代替として使用されるべきではありません。薬を服用する前には、必ず医師または他の医療専門家に相談してください。ここに記載されている情報は変更される可能性があり、すべての可能な用途、指示、注意事項、警告、薬物相互作用、アレルギー反応、副作用を網羅することを意図しているわけではありません。特定の薬物または薬物の組み合わせに関する警告や情報が記載されていない場合でも、その薬物や組み合わせがすべての患者やすべての用途において安全、有効、適切であることを意味するものではありません。
